
Las enfermedades raras pueden afectar a cualquier persona en cualquier momento de su vida. Existen más de 5000 enfermedades raras que afectan hasta casi un 10% de la población mundial. Sin embargo, solo una pequeña minoría de estas enfermedades raras tiene tratamiento. Las estimaciones varían respecto a cuántas enfermedades raras (ER) existen.
Esto es, en parte, porque los países definen de manera diferente estas enfermedades. En este artículo, hablaremos sobre Diagnóstico genético preimplantacional y enfermedades raras debido a que este 28 de febrero se conmemora al Día Mundial de las Enfermedades Raras.
-
- En los países de la Unión Europea (UE), toda enfermedad que afecta a menos de 5 personas por cada 10.000 se considera rara (Dirección de Salud Pública de la Comisión Europea) (5).
- La mayoría de los pacientes padecen enfermedades que afectan a uno de cada 10.000 habitantes o menos (Agencia Europea del Medicamento) (1).
No existe una definición única y ampliamente aceptada de enfermedad rara. La Comisión Europea de Salud Pública establece como raras a aquellas «enfermedades, incluidas las de origen genético, que son crónicamente debilitantes o potencialmente mortales. Estas enfermedades tienen tan poca prevalencia que se necesitan esfuerzos especiales combinados para combatirlas” (5).
Las enfermedades raras van de la fibrosis quística y la hemofilia al síndrome de Angelman, con una incidencia de aproximadamente 1 caso por 15.000 habitantes, y al síndrome de trigonocefalia de Opitz, que es extremadamente raro, con un caso por millón de habitantes (4).
La prevalencia de la ER dependerá de la región que estudiemos. Por ejemplo, la fibrosis quística, que es una enfermedad rara en Asia, pero común en Europa, y también de la población estudiada, como sería el cáncer en población infantil.
FACTORES GENÉTICOS
La mayor parte de las enfermedades raras tienen origen genético (el 80% del total) (7,8) y, por ende, crónicas: resultado de infecciones, alergias e intoxicaciones, o debido a causas degenerativas y proliferantes; por efectos de la exposición ambiental durante el embarazo, o después de nacer, frecuentemente, en combinación con susceptibilidades genéticas (8).
Entre las que podemos destacar las siguientes ER:
1.1 Síndrome de Arnold-Chiari (tipo 1):
Supone un descenso de una parte del cerebelo y, en ocasiones, de casi su totalidad por el agujero occipital mayor (Foramen magno), comprimiendo así el tronco encefálico. Estudios de agregación familiar (incluyendo gemelos concordantes y trillizos monocigóticos) sugieren un origen genético común en la malformación de Chiari tipo 1 (11). Una variante del Síndrome Crouzon (subtipo más frecuente de craneosinostosis) se asocia con el Síndrome Chiari tipo I y con hipertensión venosa intracraneal. Estudios recientes demuestran que mutaciones en tres de los cuatro genes de FGFR conocidos son responsables de las craneosinostosis (Crouzon, Apert, Pfeiffer y Jackon-Weiss)(6,16).
Los estudios de Meyers GA et al., 1995 y Mulliken JB et al., 1999(12), demostraron que la Chiari tipo I e hipertensión venosa intracraneal presentan una mutación específica en el exón 10 del locus FGFR3 (Ala391Glu).
Sin embargo, Fujisawa et al.,2002(5), demostraron que sería una mutación exón IIIa, exón IIIc de locus FGFR2, Tyr281Cys, síndrome de Crouzon familiar estaba asociado a Chiari I y Siringomielia (2).
1.2 Linfangioleiomiomatosis:
Enfermedad típica de mujeres en edad reproductiva, excepcional en hombres y niños: proliferación de células musculares lisas anómalas en las paredes de las vías aéreas, los vasos sanguíneos y los vasos linfáticos de los pulmones.
Las mutaciones en el gen TSC1 o, más comúnmente, el gen TSC2, causan LAM. Los genes TSC1 y TSC2 proporcionan las instrucciones para hacer las proteínas hamartina y tuberina, respectivamente (14).
1.3 Paraplejia espástica hereditaria
Se trata de un trastorno neurodegenerativo caracterizado por una espasticidad progresiva e hiperreflexia de las extremidades inferiores. La HSP puede heredarse de forma autonómica dominante, autosómica recesiva o recesiva ligada al cromosoma X, presentándose múltiples formas recesivas y dominantes (3). Solo se han identificado 11 genes autosómicos y 2 ligados al X, por lo que la base genética concreta para la mayoría de las HSP está aún por determinar (13).
1.4 Ataxia de Friedreich
Enfermedad neurodegenerativa que causa deterioro progresivo del cerebelo y ganglios espinales dorsales. Esta es una enfermedad hereditaria con un patrón de herencia autosómica recesiva. Las mutaciones en el gen FXN (cromosoma 9) y la expresión gen genera frataxina (parece ser importante para la función normal de las mitocondrias) (9).
1.5 Quiste de Tarlov
Se trata de la enfermedad de la presencia de quistes llenos de líquido cefalorraquídeo en las raíces nerviosas, localizados principalmente en la zona sacra de la columna vertebral, causando radiculopatía dolorosa (11). Es una enfermedad vinculada a un defecto genético, patologías como Ehler-Danlos, Marfan, Chiari, pero, sobre todo, de la espina bífida (polimorfismos en el gen MTHFR) y defectos en los genes del colágeno -que se expresan en la inmensa mayoría de los cromosomas y tienen múltiples expresiones- (15).
1.6 Síndrome de Prader Willi
Por lo general, de naturaleza compleja y con diversas causas y manifestaciones: Obesidad, talla baja, hipogonadismo, criptorquidia y alteraciones en el aprendizaje tras una etapa de hipotonía muscular pre y posnatal, además de una discapacidad intelectual de leve a moderada (10).
La genética de la enfermedad es bastante compleja, y es un ejemplo clásico de lo que se conoce como impronta genética. Está asociada a la pérdida de la función de varios genes en el cromosoma 15. Los genes que proporcionan instrucciones para generar los ARN nucleolar (snoRNAs). Diferentes estudios sugieren que la pérdida de un grupo particular de genes snoRNA, conocido como el clúster SNORD116 puede jugar un papel importante en la causa de los signos y síntomas del síndrome de Prader-Willi.
ENFERMEDADES RARAS Y LAS TECNICAS DE REPRODUCCION ASISTIDA
Las enfermedades genéticas en general son graves, sin existo en prevención o tratamiento satisfactorio. Por lo que las únicas vías de posible tratamiento son:
1. Prevención: consejo genético a la población de riesgo y diagnóstico prenatal y/o preimplantatorio cuando sea posible.
2. Consejo Genético: proceso de comunicación mediante el cual se obtiene información sobre:
a. Riesgo de aparición (ocurrencia)
b. Riesgo de repetición (recurrencia)
El Diagnóstico Genético Preimplantatorio (DGP) es la técnica que permite conocer la dotación cromosómica o génica del preembrión antes de ser transferido al útero y evitar la interrupción del embarazo. Esta técnica puede ser susceptible de ser realizada: 1. Preconcepcional, o 2. Preimplantaciaonal
1. Preconcepcional. Análisis cromosómico o génico del primer corpúsculo polar del ovocito. Indicaciones: mujeres de edad avanzada, o mujeres portadoras de anomalías estructurales.
2. Preimplantacional. Análisis cromosómico de una o varias blastómeras del preembrión/blastocisto.
Indicaciones: parejas con elevado riesgo trasmitir anomalías cromosómicas o génicas, a la descendencia.
Dependiendo del diagnóstico, la técnica de biología molecular utilizada, para el análisis genético del embrión, son las siguientes:
1. Reacción en cadena de la polimerasa (PCR), permite detectar mutaciones puntuales en enfermedades monogenéticas.
2. Hibridación “in situ” fluorescente (FISH):
a) selección de embriones libres de enfermedades ligadas a caracteres sexuales;
b) estudio de anomalías cromosómicas numéricas (haploidía, triploidía, nulisomías) y estructurales (traslocaciones e inversiones).
Debemos destacar que las enfermedades raras genéticas más prevalentes son la gran mayoría enfermedades monogenéticas: Síndrome de Arnold-Chiari, gen FGFR3 (cromosoma 4) y gen FGFR2 (cromosoma 9)… Herencia autosómica recesiva; Ataxia de Friedreich, gen FXN (cromosoma 9)… herencia autosómica recesiva; Quiste de Tarlov, gen MTHFR… Herencia autonómica dominante; Linfangioleiomiomatosis, gen TSC1 (cromosoma 9 (9q34)) y el gen TSC2 (cromosoma 16 (16p13)).. herencia ligada al sexo; Paraplejía espástica hereditaria, herencia ligada al sexo; otras anomalías génicas/cromosómicas: Síndrome de Prader Willi, deleción de varios genes (cromosoma 15)… Impronta genómica(16).
Las anomalías cromosómicas se relacionan con la morfología embrionaria. Existen dos tipos de anormalidades cromosómicas en el embrión:
- Las que ocurren durante la meiosis: Aneuploidias
- Las que ocurren tras la meiosis: mosaicismo, poliploidía y haploidía.
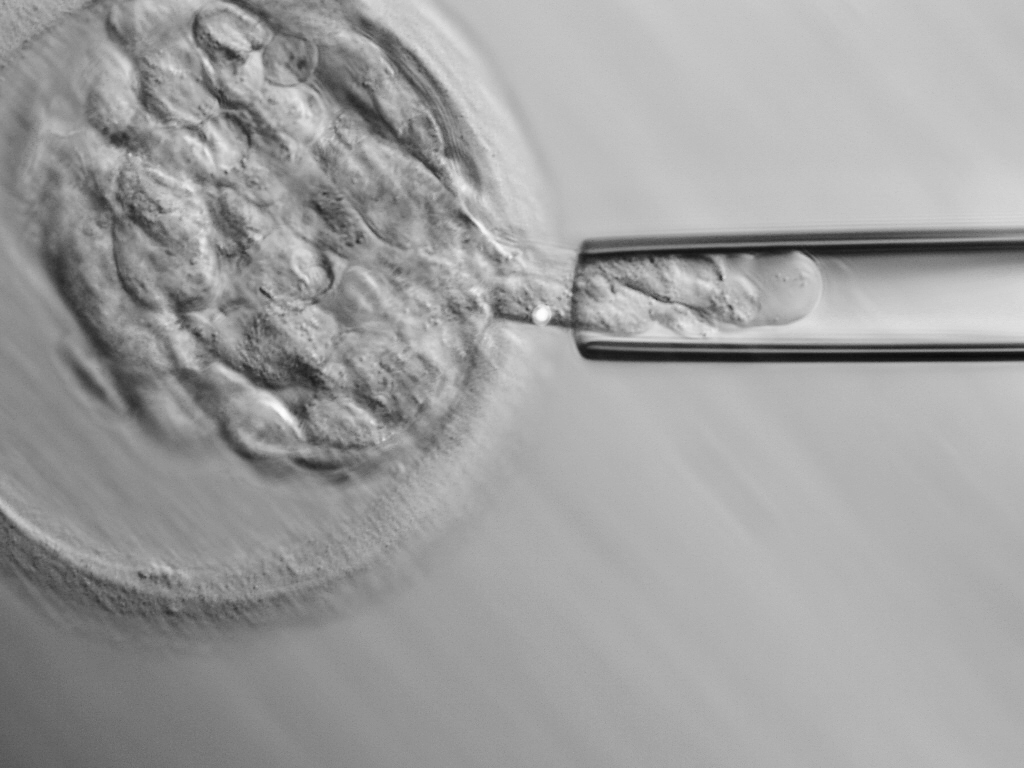
Es necesario tener en cuenta que la morfología es una herramienta válida para solo algunas anomalías cromosómicas. Por ello, el mejor método de selección será el diagnóstico genético preimplantatorio y la morfología embrionaria. Según Rubio et al, 2007(18), la tasa de desarrollo hasta blastocisto está influenciada por las posibles alteraciones cromosómicas, observándose: Euploides…66%, Trisomías…37%, Monosomías…9%, Poliploidias…21%, Haploides…0%, Mosaicos diploides…13%.
El algoritmo para la selección embrionaria en pacientes con ER susceptibles de Diagnóstico Genético Preimplantacional, podría definirse:
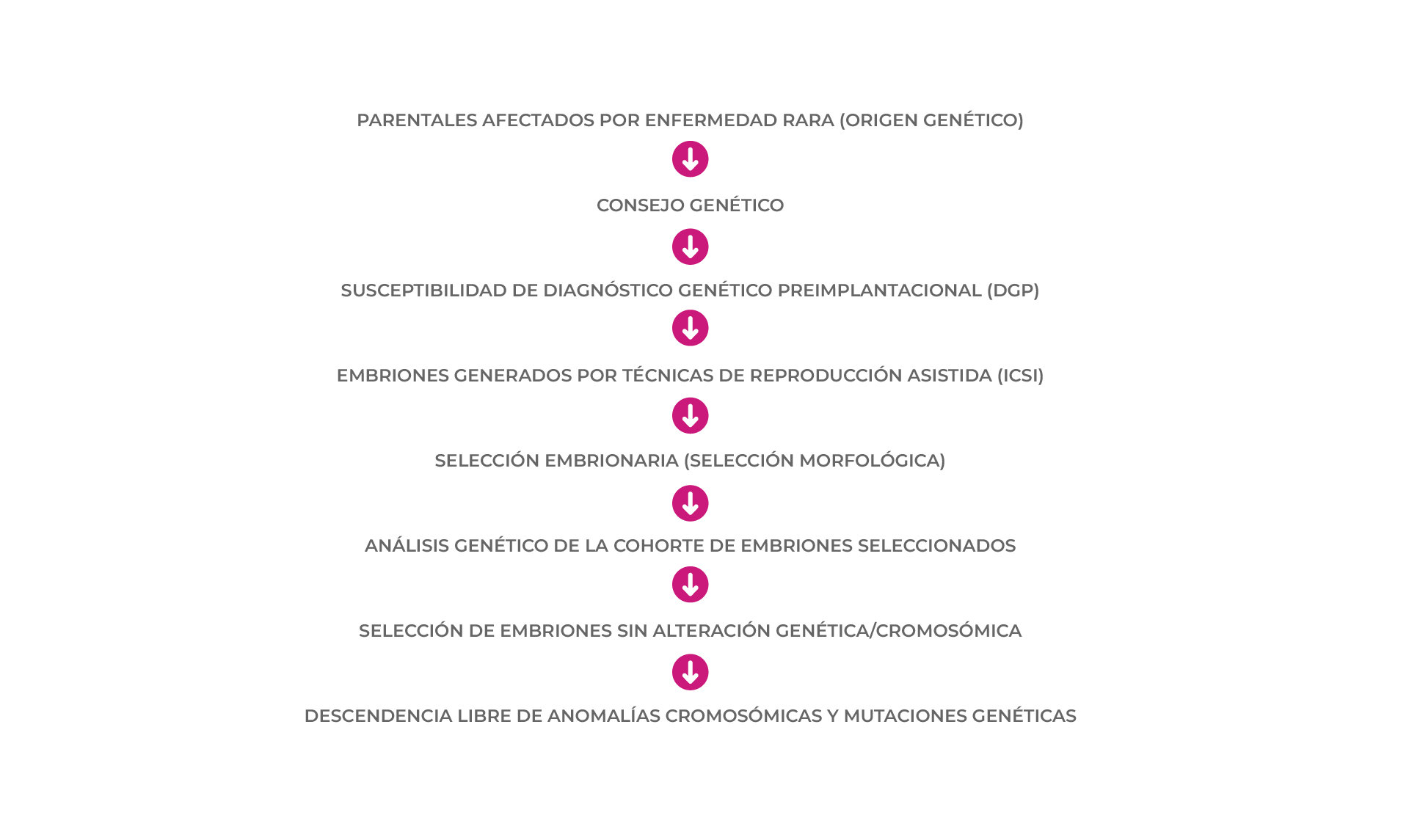
CONCLUSIONES
- El cultivo prolongado permite realizar selección embrionaria (preembriones con alto poder de implantación) pero no exentos de anomalía cromosómica.
- La combinación de selección embrionaria y el Diagnóstico Genético Preimplantacional resulta de gran utilidad en pacientes con ER.
- El DGP permite obtener preembriones libres de anomalías cromosómicas y mutaciones genéticas.



